1 - الفكرةُ الرئيسة: أوضِّحُ المقصودَ بكلٍّ منَ الآتي:
♦ المخلوط المُتَجانِس: يتكون من مادتين أو أكثر لا يحدث بينهما تفاعل كيميائي حيث تنتشر جسيمات المذاب بشكل منتظم ومتماثل في جميع أنحاء المذيب.
♦ المخلوط غير المُتَجانِس: يتكون من مادتين أو أكثر من المواد النقية لا تمتزج مكوناتها امتزاجا تاما حيث تحتفظ كل منها بخصائصها الكيميائية وتبقى في المخلوط متمايزة عن غيرها من المكونات.
♦ الذائبيّة: أكبر كتلة من المذاب التي يمكن أن تذوب في 100g من المذيب(الماء) في درجة حرارة معينة. أو كمية المذاب اللازمة لعمل محلول مشبع عند درجة حرارة معينة.
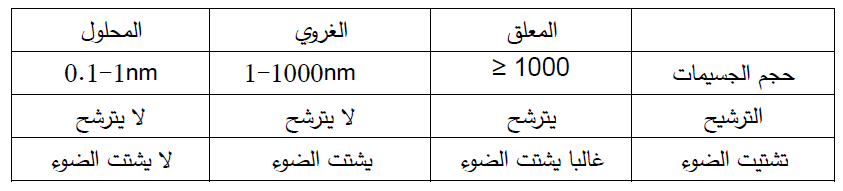
2 - أُقارنُ بين جُسيماتِ المخلوطِ المُعَلَّقِ والمخلوطِ الغَرَوِيِّ والمحلول، من حيثُ: حجمُها، وفصلُها بالترشيح، وتشتيتُها الضَّوءَ.
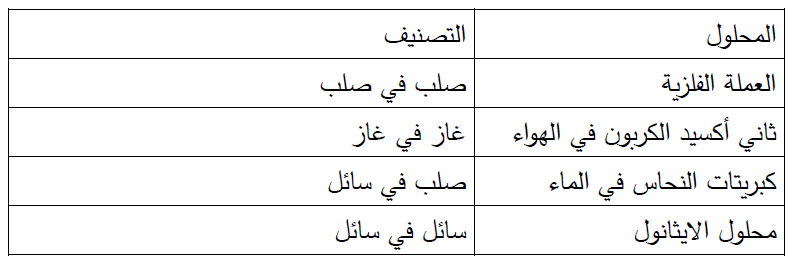
3 - أُصَنِّفُ المحاليلَ الآتية تبعًا لحالة المُذيب الفيزيائيّة إلى محاليلَ صُلبة، وسائلة، وغازيّة:
العملةُ الفِلِزيّة، ثاني أُكسيد الكربون في الهواء، كِبريتاتُ النُّحاس في الماء، محلولُ الإيثانول.
4 - أُفَسِّرُ أيُّ الغازين؛ O2 أم NH3 أعلى ذائبيّةً في الماء عند الظروف نفسِها.
NH3 لأنه يتفاعل مع الماء بسبب خواصه القطبية وفق المعادلة:
يلاحظ من المعادلة أنه ينتج أيونات موجبة وأيونات سالبة تنتشر بين جسيمات الماء فينشأ تجاذب معها.
5 - يبيِّنُ الجدولُ الآتي ثلاثةَ غازات وَكُتَلَها الموليّةَ عند الظروف نفسِها منَ الضغط ودرجة الحرارة.

أ . أُحَدِّدُ الغازَ الذي له أعلى ذائبيّةٍ في الماء. B
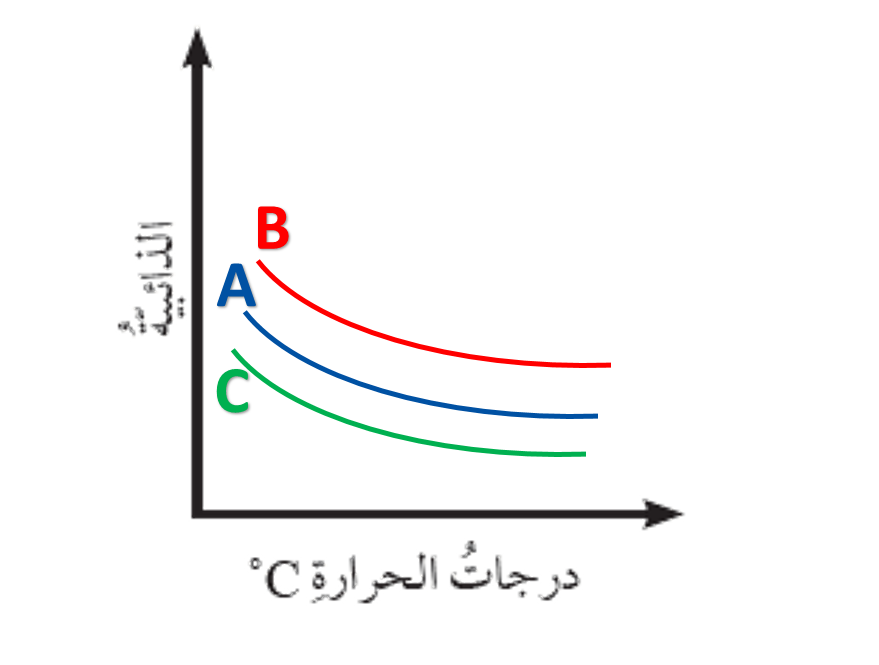
ب . أرسمُ ثلاثةَ مُنحنياتٍ تمثِّلُ ذائبيّةَ الغازات الثلاثة عند درجات حرارة مختلفة.
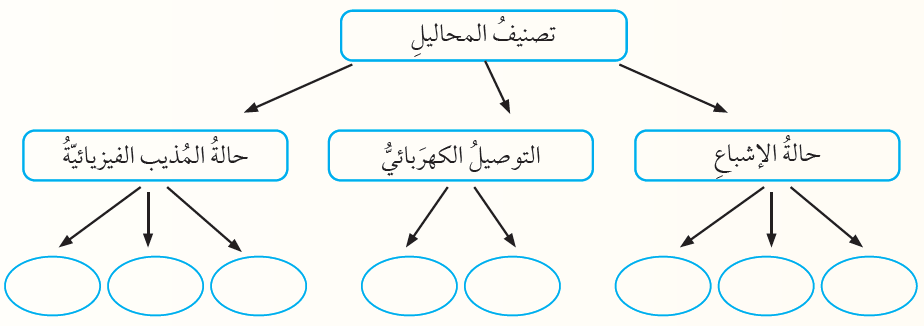
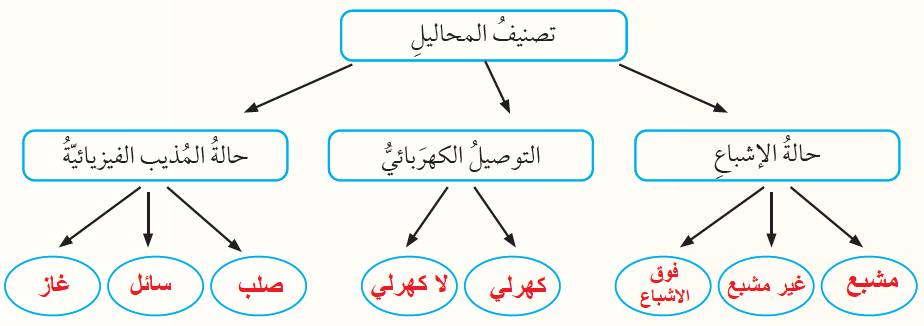
6 - أُكمِلُ المُخَطَّطَ المفاهيميَّ الآتي: